医生命システム専攻
医生命システム専攻の特色
ヒトを一つの生命システムと捉えた視点から生命現象を研究し、システム制御系の不調から生じる様々な疾病の解明と、その予防・治療方法の開発を目指します。
教員紹介
医生命システム専攻の教員は、教員紹介(医生命システム専攻)でご案内しています。
研究トピックス
分子生命分野
分子生命化学研究室
当研究室では、独自に開発した技術を用いて、近年猛威を奮う腸管出血性大腸菌O157やインフルエンザウイルスなどの新興再興感染症、さらに癌や骨粗鬆症などの各種重要疾患に対する治療薬開発を推進していく。また細胞生物学的、分子生物学的手法を用いて、方向性のある細胞内小胞輸送の分子機構の解明や、細胞内オルガネラにおける情報伝達機構など、ユニークな視点から生命現象の解明を目指す研究も積極的に進めていく。
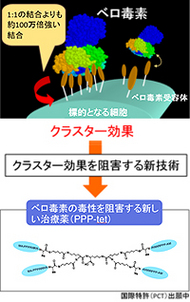
新技術で、O157感染症治療薬開発に成功。
O157などの腸管出血性大腸菌(STEC)による感染は、下痢、出血性大腸炎になるばかりでなく、ときに溶血性尿毒症症候群、脳症などの生命に関わる重篤な合併症を併発します。本感染症の主な病原因子はSTECが産生するベロ毒素です。ベロ毒素は標的細胞に存在する受容体Gb3に結合します。このときベロ毒素は一度に複数のGb3と結合することで非常に強く標的細胞に結合します。これをクラスター効果と言います。医生命システム学科は、クラスター効果を阻害する新技術を開発し、ベロ毒素の毒性をシャットアウトする新しいO157感染症治療薬(PPP-tet)の開発に成功しました。さらに、この技術を応用し、現在大きな問題となっている各種新興再興感染症・がん・炎症性疾患等に対する治療薬開発に取り組んでいます。
予防健康医学研究室
生活習慣病の一次予防に有用な疾病予防バイオマーカーを同定するために、生活習慣病発症動物モデル(糖尿病発症マウス、糖尿病性腎症発症マウス、動脈硬化促進マウスなど)を用い、得られた血液検体を京都府立医科大学と共同研究で、網羅的蛋白解析に付している。またこれらモデルを用いて、漢方薬、各種薬剤、機能性食品の生活習慣病発症抑制効果を検討している。
抗加齢医学研究室
アンチエイジングリサーチセンター/糖化ストレス研究センター(オリジナルサイト)
抗加齢医学の観点から健康増進と健康長寿を目的として、検査法・評価法・指導法・データベース構築法・データ解析法に関する研究を行っている。これまで作成したシステムは企業検診や地域検診にて導入されつつある。今後このような動きが国内で広がると予想され、収集されるデータのデータベースの構築、その解析方法の確立が今後の課題となっている。

歩数計を使った脱・メタボ計画。
40歳以上の男性は2人に1人、女性は5人に1人がメタボリックシンドロームまたはその予備軍だと言われています。予防や改善のため、各地域では運動教室などの対面式運動指導が行われていますが、場所や指導者の確保が難しいという問題があります。そこで、医生命システム学科では、非対面式でも運動指導が行えないかと、歩数計と郵送物を使ったアプローチを検証。歩数計から運動量データを毎月取得・分析し、次月の目標数値を記載したシートを被験者に郵送しました。約4ヶ月の検証の結果、この方法は中高齢者の健康維持に有効だとわかりました。続けて、肉体年齢を算出し、具体的に何歳若返ったか伝えるなど、健康へのモチベーションを高める方法を研究しています。
神経科学分野
神経病理学研究室
歳をとると大多数のヒトが脳内に老人斑と神経原線維変化という病変をもつようになる。これらの病変の密度が高くなった状態がアルツハイマー病である。老人斑は、βタンパクとよばれるタンパク質から、神経原線維変化はτ(タウ)というタンパク質から構成されている。我々の研究室では、βタンパクを産生するγセクレターゼ及び、タウに焦点を絞って研究を進め、近い将来アルツハイマー病のバイオマーカー探索も始める予定である。
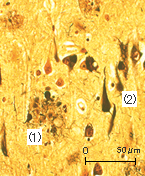 アルツハイマー病の病変
アルツハイマー病の病変多数の老人斑(1)と
神経原線維変化(2)
アルツハイマー病の原因を探る。
ヒトは年をとると脳内に病気による生体の変化(病変)が現れやすくなります。病変の密度の高くなった状態がアルツハイマー病です。アルツハイマー病は加齢と密接な関係があり、80歳以上で患者数は急激に増加します。日常生活でアルツハイマー病の患者さんを見かけることが多くなったのは、日本の平均寿命が延びて80歳を超える方が多くなったためです。脳の病変とは老人斑と神経原線維変化と呼ばれているものです(写真参照)。医生命システム学科では、これら2つの病変がどのようにして出来るのかを、様々な材料を用いて研究します。
神経生理学研究室
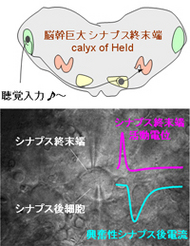 脳幹・聴覚伝導路の神経回路図
脳幹・聴覚伝導路の神経回路図
情報伝達のカギ、シナプスに迫る。
脳の情報伝達制御の要を担うシナプス。その情報伝達のメカニズムを解明することは、脳研究の最重要課題です。医生命システム学科は、シナプスの形成から機能が成熟・分化するまでの過程で、シナプス特性の変化とタンパク質の発生や消滅が同時に起こるという事実に注目。分子・機能間の因果関係を解くことが、謎の解明につながると考えています。その第一歩として、生後様々な時期のネズミの脳幹を取り出し、生きた状態の神経細胞とシナプスを観察。電極を使って細胞内記録を行い、巨大神経終末端と後細胞から同時に電気信号を記録することに成功しました。
細胞代謝化学研究室
脊椎動物の身体支持やカルシウム調節において重要な役割をもつ骨は、単なる無機的な構造物ではなく、常に’形成’と’破壊’を繰り返すことで新陳代謝する組織です。骨を壊す「破骨細胞」と骨を作る「骨芽細胞」は互いにバランスをとって働くことで、骨の強度が適切に保たれています。これに対して、老化や閉経によって生じる異常な破骨細胞の活性化や骨芽細胞の機能低下は、骨量低下を引き起こすことで骨折のリスクを高める骨粗鬆症の原因となります。本研究室では、①破骨細胞形成にかかわる新たな仕組みを理解すること、②得られた知見を活かして破骨細胞を阻害する化合物を探索することで、骨粗鬆症に対する新しい予防・治療手段を見つけ出すことを目的としています。
システム生命分野
システム生命科学研究室
システム生命科学研究室(オリジナルサイト)
ヒトをはじめ生物にとって酸化反応は重要な反応系である。その一方で、酸化ストレスは様々な病気の原因となり、老化を促進させる。当研究室では生物に起こる生命現象をシステムとして捉え、これらのメカニズムを解明し、酸化ストレスを制御することにより、ヒトが本来もつ適応能力を最大限に引き出す方法を探究する。
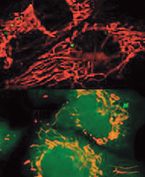 ヒト血管内皮細胞のミトコンドリア(上図赤色)と、
ヒト血管内皮細胞のミトコンドリア(上図赤色)と、酸化ストレス時の活性酸素(下図黄色)
酸化ストレスと病気。
私たちの体の中には活性酸素を除去する抗酸化システムが存在し、活性酸素の生成と除去がバランスをとった状態にあります。このバランスが崩れ活性酸素による酸化が亢進した状態が、酸化ストレスです。酸化ストレスは様々な病気の原因となり、老化を促進させる一方で、酸化反応は細胞内のシグナル伝達に機能したり、体の防御機能を高める良い作用をもちます。システム生命科学研究室では、酸化ストレスをキーワードに神経変性疾患や糖尿病の発症メカニズムを明らかにする研究を行っています。病気のメカニズムを明らかにすることにより、新しい治療法や予防法の開発、病態を示すバイオマーカーが同定されると期待されます。
遺伝情報研究室
ストレス応答や代謝調節などの恒常性維持機構において、シグナル伝達機構と遺伝子発現制御機構の解明を目指し、ノックアウトマウスを用いた発生工学ならびに生化学・分子生物学的手法により解析する。さらに、これら制御機構の破綻がもたらす疾患の発症機構の理解と治療法の創出も試みる。
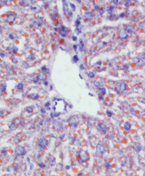 脂肪肝モデルマウスの肝臓。
脂肪肝モデルマウスの肝臓。おびただしい脂肪の蓄積が見られる(赤)
遺伝子の発現調節から疾患の原因を探る。
生命現象は、ほとんどタンパク質に制御されていると言っても過言ではありません。タンパク質は、DNAからmRNAを介して合成されます。これは遺伝子発現と呼ばれ、この過程ではタンパク質が必要な時に必要な量だけ、必要とする細胞で発現するように厳密に制御されています。一方、病気の原因は様々ですが、その一つに遺伝子発現の異常が考えられます。医生命システム学科では、このような遺伝子発現の異常がもたらす疾患の発症メカニズムを探るため、ノックアウトマウスなどの疾患モデルを用いて研究しています。